
ТЕЗИСЫ ДОКЛАДОВ XII ВСЕРОССИЙСКОЙ КОНФЕРЕНЦИИ РЕФЛЕКСОТЕРОПЕВТОВ
38
РЕФЛЕКСОТЕРАПИЯ И КОМПЛЕМЕНТАРНАЯ МЕДИЦИНА
№ 4 (26) 2018
гноз» в значительной степени потеснил на За-
падном рынке «аборигенные» методы. Не под-
лежит сомнению, что одной из составляющих
данного феномена является фундаментальный
научный базис, легший в основу этой разработ-
ки, который могло себе позволить в своё время
только государство с плановой экономикой.
Обоснование (актуальность)
исследования
При разработке вышеозначенной научной те-
матики была поставлена «сверхзадача»: получать
максимально комплексные результаты о состоя-
нии здоровья человека при минимальных ресурс-
ных (временных, квалификационных) затратах.
К тому же значимым фактором являлась эффек-
тивность функционирования разрабатываемой
методики диагностики в составе автоматизи-
рованных информационных систем контроля
за состоянием человека (в том числе и в режиме
реального времени). Данные предпосылки за-
ставили обратить внимание на анализ различных
параметров кожного покрова и их связи с вну-
тренними процессами функционирования орга-
низма. В результате многочисленных натурных
экспериментов была подтверждена целесообраз-
ность данного подхода.
Цель и задачи исследования
Дальнейшее развитие ЭПД «Прогноз» прохо-
дило в рамках международного сотрудничества.
И здесь была с успехом реализована концепция
сочетания Российских инноваций и технологи-
ческих возможностей ЕС и Германии, в част-
ности. К тому же таким образом авторы смогли
удовлетворить свои творческие амбиции, реали-
зация которых стала затруднительной в рамках
переходного периода Российской государствен-
ности. Таким образом, фирмой MEDPREVENT
systems GmbH & Co. KG была зарегистрирована
торговая марка Prognos® и поставлена цель по-
лучить на основе вышеназванных научных раз-
работок продукт для рынка ЕС. Сразу надо от-
метить, что такая задача представлялась доста-
точно амбициозной, так как речь шла именно
о медицинском продукте, к которым в ЕС тра-
диционно предъявляются достаточно жёсткие
требования.
Материалы и методы
Согласно законодательству ЕС, сертифика-
ции продукций медицинского назначения осу-
ществляется через аккредитованные подраз-
деления, число которых, во‑первых постоянно
сокращается по мере ужесточения регламента
прохождения тестирования, во‑вторых у этих
организаций имеется определенный рейтинг,
который значим для дальнейшего продвижения
на рынок. Так сертификацией продукцииMED-
PREVENT systems занимается британская фир-
ма BSI, имеющая сигнатуру «By Royal Charter»
(Королевский патент), что является призна-
ком наивысшего качества оказываемых услуг.
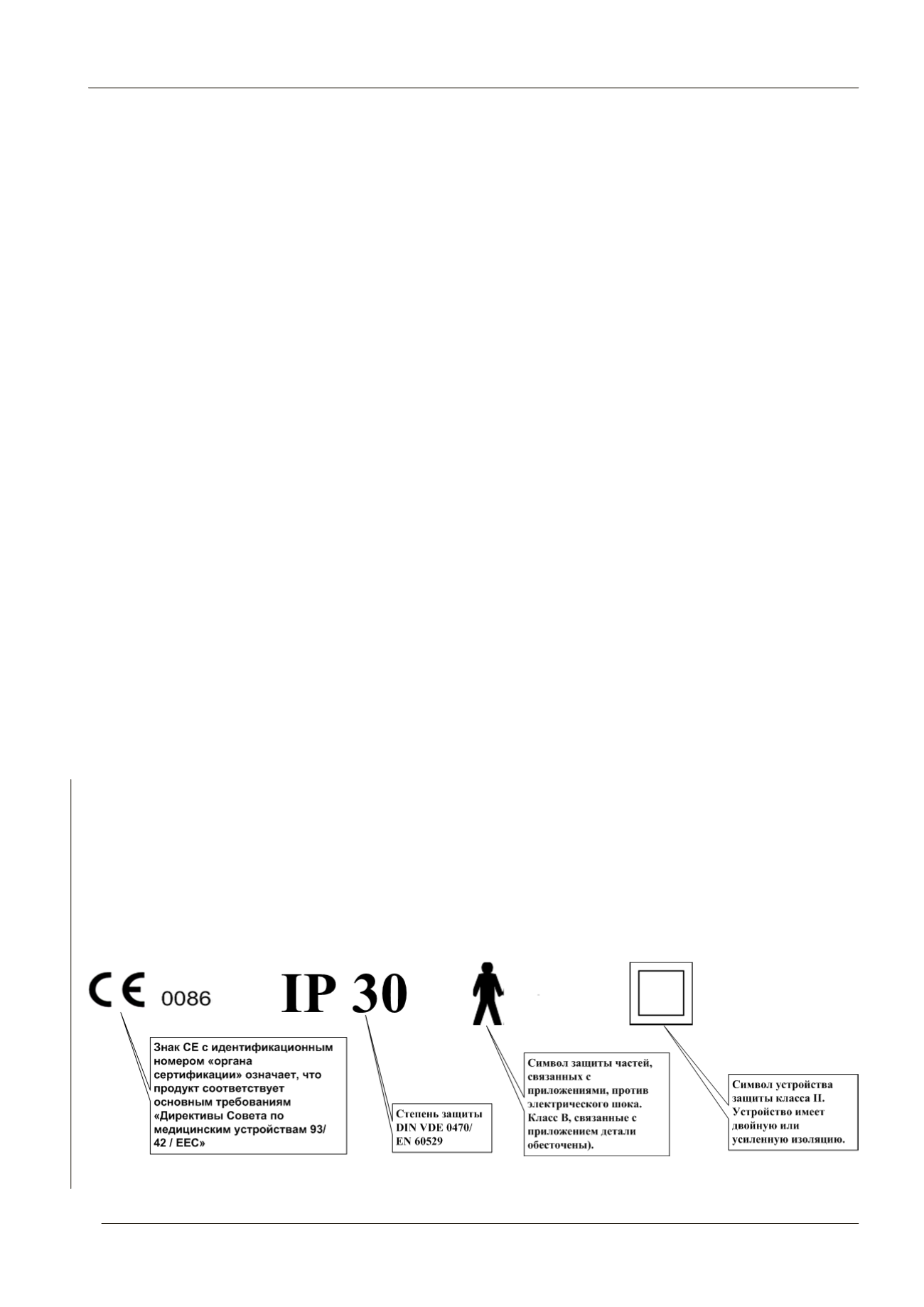
Отдельно сертифицируются измерительные
средства, которые для медицинских продуктов
должны иметь маркировки, представленные
на рис. 1.
К программному обеспечению (ПО) ме-
дицинской технологии также предъявляются
жёсткие требования. В частности, оно должно
сопровождаться достаточно объемным доку-
ментом «Клиническое описание», в котором
в обязательном порядке должен присутствовать
раздел с указанием научных исследований, вы-
полненных при помощи указанного аппарат-
но-программного комплекса [1]. Также должны
быть представлены отчёты о различных вари-
антах клинического использования, в соот-
ветствии со стандартной формой, содержащей
в частности разделы: «Область применения»,
«Результаты» и «Непредвиденные результаты».
Рис. 1.
Признаки сертификации продукта по Европейским стандартам










